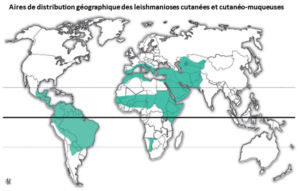
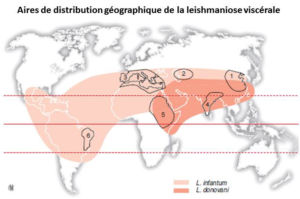
Diagnostic biologique
Le CNRL en collaboration avec le département de Parasitologie-Mycologie du CHU de Montpellier réalise en routine :
- le diagnostic biologique des leishmanioses
- l’identification moléculaire des différentes espèces de Leishmania
- Le diagnostic sérologique
1 . Envoi d’un échantillon biologique pour le diagnostic ou l’identification moléculaire
Nature de l’échantillon :
- pour la leishmaniose viscérale, sang ou moelle osseuse
- pour les leishmanioses tégumentaires, biopsie, grattage, curetage de lésions cutanée ou muqueuse.
PROCÉDURE DE RECUEIL, DE CONSERVATION ET D’ENVOI DES ÉCHANTILLONS
Stockage et envoi des échantillons à +4 °
Sang veineux périphérique
5 ml de sang veineux sur tube SST pour recherche d’anticorps
5 ml de sang veineux sur tube EDTA pour recherche par PCR
Moelle osseuse
0,5 ml de MO sur tube EDTA pour recherche par PCR
Sont acceptables selon le type de lésion et les habitudes de prélèvement :
- grattage cutané ou muqueux sur le pourtour de la lésion à l’aide d’une curette
- écouvillonnage appuyé sur écouvillon sec
- ponction/aspiration de la lésion
- biopsie cutanée ou muqueuse
Il est important que les échantillons soient stockés et expédiés à 4°C dans un tube stérile contenant une ou deux gouttes de sérum physiologique stérile afin d’éviter la dessication.
Tout autre type d’échantillon (frottis sur lame, bloc anapath, etc.) peut potentiellement être analysé
Si possible indiquer le ou les pays éventuels de contamination
| Ajouter la fiche de demande de diagnostic et/ou de typage complétée avec le plus de précision possible.
| Adresser à : PEB Site Unique de Biologie 371 Avenue du Doyen Gaston Giraud 34090 Montpellier CEDEX 5 Pour d’éventuelles questions : Département de Parasitologie-Mycologie, CHU de Montpellier tel : 04 67 33 23 76 Email : cnr-leishmania |
2 . Envoi d’une souche pour typage
(préciser s’il s’agit d’une demande pour la prise en charge d’un patient ou d’une demande d’intérêt scientifique)
– conditionnement de la souche (surnageant de milieu diphasique type NNN, ou milieu de culture liquide) en tube Nunc ou en boite de type Falcon,
– envoi en emballage avec triple enveloppe selon la réglementation en vigueur.
| Ajouter la fiche demande de typage d’une souche en culture complétée avec le plus de précision possible.
Ne pas oublier, pour l’isoleur d’attribuer un sigle à la souche | Département de Parasitologie-Mycologie, CHU de Montpellier CNR des Leishmanioses 371, Avenue du Doyen Gaston Giraud 34090 Montpellier tel : 04 67 33 23 76 fax : 04 67 33 77 93 Email : cnr-leishmania |